Que la dosis de levotiroxina sea 100% eficaz va a depender de ciertos factores conductuales, farmacológicos y patológicos que interfieren en esta.
A pesar de un intento tras otro de ajustar la levotiroxina (T4), un número muy, muy alto de pacientes no logra mostrar una respuesta química y / o clínica completa a esta dosis pautada de T4.
Cada año me suben el eutirox y sigo sin mejorar… claro pero, ¿cuánto de ese eutirox estás absorbiendo?
No me voy a centrar en lo de separar el eutirox 3 horas del café o de la comida, sino en casos en los que las pacientes no absorben ni un 50% de eutirox.
Si ya tenemos elementos “ladrones de tirosina” , te dejo el link del artículo y léelo un par de veces -> https://mariapowerpt.com/ladrones-de-tirosina/ pues imagínate si encima, absorbes el 50% del eutirox que te recetan…
La T4 se absorbe esencialmente en el intestino delgado.
Se ha demostrado que la absorción de T4 se reduce significativamente cuando el fármaco se toma después de una comida. De hecho, se ha demostrado que ciertos alimentos o bebidas ( p . Ej. , Fibras dietéticas, soja, café o frutas) reducen la absorción de T4.
En ayunas, los valores máximos de absorción de T4 ocurren en los primeros 90 minutos después de la administración de T4, con un rápido aumento en los primeros 60 minutos.
El tiempo para alcanzar la concentración máxima (T max ) de T4 es ~ 2 horas después de la ingestión de T4. Poco después, la absorción comienza a estabilizarse.
En un estudio con sujetos hipotiroideos,
- el tiempo máximo de absorción fue de 3 horas,
- después de una comida, el valor máximo de absorción de T4 disminuye y el tiempo máximo se retrasa, con la consiguiente disminución de la biodisponibilidad de T4,
- cuando la comida no se pospone al menos 1 hora después de la ingestión de T4, puede producirse un retraso y una disminución de la absorción intestinal de T4,
- sin embargo, la ingesta de T4 antes de acostarse mejoró significativamente la eficacia de la hormona tiroidea, probablemente porque la menor motilidad intestinal durante la noche aumenta el tiempo de exposición de T4 a la mucosa intestinal o por un mejor cumplimiento del tratamiento por parte del paciente.
A pesar de estos estudios, los folletos sobre esta hormona todavía indican un lapso de tiempo de 30 minutos entre la ingestión matutina de T4 y el desayuno, y los médicos que prescriben suelen recomendar el mismo intervalo.
Algunas condiciones de vida pueden estar asociadas con variaciones en la tasa de absorción de T4. En particular, durante el embarazo, el aumento de la progesterona provoca un retraso en el vaciamiento gástrico y un tiempo de tránsito del intestino delgado prolongado en ~ 30% a 50%. Este cambio puede contribuir al aumento general de la necesidad de T4 durante el embarazo.
Como hemos visto el vaciamiento gástrico y el tiempo de tránsito del intestino delgado influye en gran medida en la dosis de eutirox necesaria.
Este punto es el que siempre recalco a la hora de tratar la patología de la persona, un buen abordaje del sistema digestivo, sobre todo de limpieza hepática y de “puesta a punto” del intestino.
-
La absorción de T4 parece estar ligeramente disminuida en un 4% en pacientes en los que va disminuyendo su masa magra (músculo, vaya así que aquí 👈 también es importante el 💪🏾).
-
La malabsorción de levotiroxina relacionada con el estómago representa actualmente un problema cada vez más reconocido en un número importante de pacientes con hipotiroidismo.💪🏾 La maquinaria productora de ácido ( es decir , H + / K + ATPasa) se encuentra en las glándulas oxínticas del fondo gástrico y su acción se ve reforzada por la producción de gastrina a partir de las células G antrales.
-
La producción de ácido se elimina parcial o totalmente en pacientes con gastritis crónica y / o atrofia gástrica, y se bloquea en aquellos tratados con inhibidores de la bomba de protones (IBP), así como parcialmente bloqueado y contrarrestado por la producción de NH3 en pacientes con infección por Helicobacter pylori.
-
Todas estas condiciones se han relacionado con un mayor requerimiento de T4.

In vivo , se ha demostrado el papel de la secreción de ácido gástrico en pacientes tratados con bocio con alteración de la secreción de ácido gástrico. De hecho, el requerimiento diario de T4 se incrementó en un tercio en pacientes con gastritis atrófica y gastritis relacionada con H. pylori y fue máximo en aquellos con estas dos condiciones. De acuerdo con estos resultados, los pacientes con hipotiroidismo con anticuerpos anti-células parietales y anti factor intrínseco positivos mostraron un aumento en el requerimiento diario de T4.
Estos autores encontraron un aumento del 17% en los pacientes con anticuerpos anti células parietales positivo en comparación con los pacientes con PCA negativo, y tal aumento fue aún mayor (+ 32%) en aquellos pacientes con gastritis atrófica comprobada. En pacientes tratados con T4 con infección reciente por H. pylori , también se ha observado un aumento significativo de TSH. Tal efecto fue contrarrestado aumentando la dosis de T4, siendo solo parcialmente revertido por la erradicación de H. pylori. La erradicación de esta infección, de hecho, no siempre restablece las condiciones previas de la mucosa, ya que puede sobrevenir una antritis (inflamación de la parte del estómago que conecta con el intestino) incluso una pangastritis (gastritis aguda severa) con una posible evolución a atrofia gástrica. La infección por H. pylori afecta del 30% al 50% de la población general en todo el mundo y la alta prevalencia de este único trastorno puede potencialmente incrementar la necesidad de T4 en un mayor número de pacientes que en aquellos con supuesta pseudomalabsorción.
La enfermedad celíaca, gastritis atrófica, la intolerancia a la lactosa y la infección por Helicobacter pylori pueden impedir la absorción de levotiroxina.
Durante el tratamiento de estos trastornos, es necesario controlar la hormona estimulante del tiroides en suero y los valores de T4 libre para reducir el riesgo de desarrollar hipertiroidismo iatrogénico.
La soja y el café tienen el mayor impacto en la reducción de la absorción, mientras que la vitamina C tiene la capacidad de aumentarla.
Aquí el estudio 📑 William Jubiz, Marcela Ramirez, Effect of Vitamin C on the Absorption of Levothyroxine in Patients With Hypothyroidism and Gastritis, The Journal of Clinical Endocrinology & Metabolism, Volume 99, Issue 6, 1 June 2014, Pages E1031–E1034, https://doi.org/10.1210/jc.2013-4360
En este estudio 31 pacientes tomaron con la levotiroxina y el agua, 500 mg de vitamina C.
Todos los pacientes tenían patología gastrointestinal y no tenían un buen control cuando tomaban L-T 4 antes del estudio y 23 tenían tiroiditis autoinmune o hipotiroidismo idiopático.
Conclusión del estudio: en pacientes con hipotiroidismo y patología gastrointestinal, la vitamina C mejora las anomalías en las concentraciones séricas de T 4 , T 3 y TSH libres . Este enfoque es útil en el manejo de estos pacientes.
Interferencia de fármacos a nivel gástrico
Se ha descrito el efecto del omeprazol sobre las necesidades de T4 en pacientes con bocio en los que el uso de estos dos fármacos aumenta significativamente la TSH sérica.
El efecto se revirtió aumentando la dosis de T4 en un 37% o suspendiendo el uso de IBP.
Los inhibidores de la bomba de protones (IBP) son medicamentos que funcionan al reducir la cantidad de ácido gástrico producido por glándulas en el revestimiento del estómago.
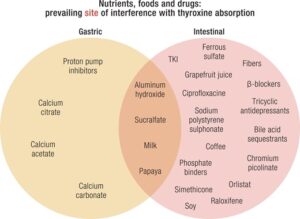
Se establece una disminución en la absorción de LT4 y es clínicamente significativa cuando se administra concomitantemente con colestiramina, colesevelam, lantano, carbonato cálcico, citrato cálcico, acetato cálcico, sulfato de hierro, ciprofloxacina, hidróxido de aluminio, sevelamer o inhibidores de la bomba de protones.
Trastornos intestinales que afectan la absorción de T4
La enfermedad celíaca (EC) tiene una prevalencia estimada en la población general del 1% ( 135 ) pero su prevalencia asciende al 2-5% de los pacientes que además padecen una patología autoinmune tiroidea, principal causa de hipotiroidismo.
Además, dado que la enfermedad autoinmune tiroidea es el trastorno autoinmune más frecuente, se puede detectar una tasa definida más alta de tiroiditis de Hashimoto en pacientes con EC que en la población general.
La presencia conjunta de estas dos enfermedades es una de las asociaciones más frecuentes incluidas en el síndrome autoinmune poliendocrino tipo 3B. La proporción entre pacientes con EC manifiesta y pacientes en los que la enfermedad está presente pero no diagnosticada es de aproximadamente 1:8. Como la EC también puede presentarse sin síntomas gastrointestinales sugestivos (CD de presentación atípica), se debe sospechar su presencia en pacientes con hipotiroidismo con una necesidad aumentada de T4.
Hasta donde sabemos, el deterioro de la absorción oral de levotiroxina en un paciente con EC se informó por primera vez en 1993 en un paciente con alergia a la proteína de la leche y Enfermedad Celíaca. Posteriormente, algunos informes de casos confirmaron la aparición de resistencia al tratamiento con levotiroxina oral en pacientes con hipotiroidismo con enfermedad celíaca.
En 2012, dos estudios elaboraron el tema en 7 pacientes con EC no tratada y en 35 sujetos afectados por EC atípica. En ambos grupos, una dieta sin gluten revirtió el aumento de las necesidades hormonales, solo parcialmente en el primer estudio y completamente en el segundo.
Los mecanismos que conducen al aumento de la necesidad de T4 en pacientes con EC pueden seguir a la reducción progresiva de la superficie intestinal que caracteriza las lesiones histológicas de esta enfermedad: (i) acortamiento de las vellosidades hasta la atrofia total, debido a la apoptosis de los enterocitos y a la inadecuada regeneración celular en las criptas, y (ii) infiltración linfocitaria importante. Este evento, a su vez, determina la pérdida de proteínas y enzimas en el borde en cepillo, lo que dificulta la absorción de una gran cantidad de nutrientes (145 ). En pacientes con EC, el grado de deterioro de la eficacia del fármaco puede depender de las características farmacocinéticas de cada fármaco ( 146 ). De hecho, además de la reducción de la superficie absorbente, se informaron las siguientes características patológicas en pacientes con EC: aumento de la permeabilidad intestinal, aumento del tiempo de tránsito gastrointestinal y cambios en el pH luminal del intestino ( 146 , 147 ). Incluso se ha descrito vaciamiento gástrico anormal, quizás en función de una secreción alterada de colecistoquinina y del polipéptido plasmático YY, hormonas implicadas en la motilidad gastrointestinal ( 147). También se ha observado una mayor prevalencia de sobrecrecimiento bacteriano en el intestino delgado, generalmente en pacientes con persistencia clínica de los síntomas, incluso después de eliminar el gluten de la dieta ( 148 ). Al igual que otros nutrientes y fármacos, todos estos mecanismos pueden contribuir a la malabsorción de T4.
La mala digestión de la lactosa es una condición, en su mayoría asintomática, a la que están expuestos ~70% de los seres humanos adultos (lactasa no persistente). Esta condición es causada por la disminución de la actividad de la lactasa residual debido a la regulación a la baja de la enzima responsable de la hidrólisis de la lactosa a glucosa y galactosa. La intolerancia a la lactosa (IL) tiene en cambio un cuadro clínico pleiotrópico, presentándose con diarrea, distensión abdominal, flatulencia, dolor abdominal, cuya intensidad está relacionada con (i) la cantidad de lactosa ingerida, (ii) la composición microbiana intestinal, (iii) actividad motora gastrointestinal y, finalmente, (iv) la sensibilidad visceral a los productos de fermentación de la digestión de la lactosa.
Además de la forma primitiva, LI puede seguir cualquier proceso capaz de destruir la mucosa del intestino delgado ( p. ej ., EC, infecciones, cirugía). Inicialmente, Muñoz-Torres describió el caso de un paciente que mostró una necesidad aumentada de T4 inducida por LI, que se resolvió cambiando a una formulación de T4 sin lactosa e iniciando una dieta sin lactosa. Se observó un efecto similar después de 8 semanas de restricción de lactosa, lo que confirma que una dieta sin lactosa puede mejorar la homeostasis farmacológica de la tiroides en pacientes con IL. Posteriormente, un estudio sistemático confirmó la mayor necesidad de T4 en un grupo mayor de pacientes con IL, en comparación con un grupo control sin signos o síntomas de malabsorción (+31%) (43 ). Más de un mecanismo puede explicar el efecto de LI sobre la necesidad de T4. Cuando no se produce la hidrólisis de la lactosa, este azúcar se acumula y atrae agua en la luz intestinal. Así, un contenido intestinal alterado puede formar complejos con T4, impidiendo la absorción , o incluso puede aumentar la motilidad intestinal, reduciendo así la exposición de T4 a la superficie absorbente. Además, LI a menudo se asocia con el crecimiento excesivo de bacterias en el intestino delgado, lo que también puede afectar el reciclaje enterohepático de T4.
La lactosa también se usa como excipiente en algunos medicamentos y en algunas formulaciones de tabletas T4, y las cantidades no suelen revelarse en los prospectos. Este hecho hizo sospechar que el contenido de lactosa en estas preparaciones de T4 puede representar un problema: un estudio, sin embargo, proporcionó evidencia de que la ingestión de hasta 400 mg de lactosa no desencadena síntomas gastrointestinales ni afecta la prueba de aliento con lactosa. Notablemente, los síntomas gastrointestinales generalmente son provocados por cantidades >5 g de lactosa ingerida. Por lo tanto, la posibilidad de que una cantidad muy pequeña de disacárido en la tableta de T4 pueda ser responsable de su malabsorción es poco probable.
La infección parasitaria por Giardia lamblia también se ha considerado como causa de malabsorción de T4. Este parasitismo es esporádico en los países occidentales donde parece más frecuente en viajeros. Por el contrario, este protozoario flagelado suele ser endémico en ambientes caracterizados por malas condiciones sanitarias. Las manifestaciones clínicas van desde trastornos gastrointestinales graves hasta formas asintomáticas. Solo dos informes de casos han descrito una mayor necesidad de T4 debido a la infestación de G. lamblia, ambos describiendo una elevación de la TSH sérica y una mayor necesidad de T4 que se revirtieron con el tratamiento antiparasitario adecuado. La causa de la malabsorción de T4 en estos pacientes es el daño inflamatorio de la mucosa y la apoptosis epitelial inducida por el protozoo; además, en estos pacientes se puede observar un aumento de la permeabilidad intestinal debido a la disrupción de las uniones estrechas intestinales.
“Un programa ajustado de tratamiento con T4 representa un requisito previo para detectar cualquier necesidad creciente de tiroxina”.
Además de los trastornos que afectan directamente a la mucosa absorbente, las enfermedades que afectan a los órganos implicados en el proceso digestivo pueden afectar la eficacia de la T4 oral. De hecho, la insuficiencia pancreática puede causar esteatorrea luego de la reducción de la secreción de lipasa a <10% de los niveles normales. En un estudio inicial sobre ocho pacientes publicado en 1962, los autores observaron que la esteatorrea pancreática aumentaba la tasa de eliminación de la hormona, mostrando que las pérdidas fecales de la hormona eran más altas de lo normal. También se sugirió una interferencia directa con los compuestos generalmente degradados por las enzimas pancreáticas, lo que resulta en una adsorción de yodo orgánico en el contenido intestinal.
Se ha informado que la fibrosis quística que con frecuencia conduce a insuficiencia pancreática es una causa de la disminución de la absorción de la hormona tiroidea. Además, un artículo reciente describió dos casos en los que se demostró una mayor necesidad de T4 en pacientes con cirrosis hepática. Los autores especularon que la alteración de la secreción de bilis, además de la variación en la concentración de globulina transportadora de tiroxina, podría explicar este efecto. De manera similar, un estudio de Sinha y Van Middles subrayaron el papel de la bilis en la reducción de la unión de T4 a las proteínas plasmáticas intraluminales, aumentando así la absorción de T4 marcada en un asa yeyunal lavada de ratas. Los autores postularon la presencia en la bilis de sustancias que compiten por la unión de T4 con proteínas plasmáticas.
En una sección anterior, describimos el supuesto mecanismo de absorción de T4 a nivel del intestino delgado; el efecto del síndrome del intestino corto sobre la absorción de T4 se ha investigado desde la década de 1980. Esta enfermedad suele ser consecuencia de malformaciones congénitas o enfermedades adquiridas que requieren la resección quirúrgica del intestino delgado, lo que provoca una reducción de la superficie de absorción intestinal junto con alteraciones de la motilidad. Además, la ausencia del último asa ileal y de la válvula ileocecal puede hacer que las bacterias colónicas se eleven en el intestino delgado residual, produciendo un ambiente de disbiosis dominado por los lactobacilos. El estudio de la absorción de T4 radiomarcada en cinco pacientes con síndrome de intestino corto en comparación con dos sujetos sanos reveló una reducción neta de la absorción de T4 oral independientemente de la longitud del intestino intacto. Se ha sugerido que, además de la superficie intestinal acortada, el tránsito intestinal acelerado puede desempeñar un papel clave en la determinación de la malabsorción de T4 en estos pacientes.
Cirugía bariátrica
Por motivos similares, la interferencia en la absorción de T4 ejercida por la cirugía bariátrica, incluida la derivación intestinal, se ha analizado ampliamente, aunque con resultados contradictorios (ver arriba para la cirugía bariátrica que involucra solo el estómago). Los tres informes de casos sobre los efectos de la técnica de derivación yeyunoileal informaron consistentemente un aumento significativo (de tres a cuatro veces más que la dosis normal) de la necesidad de T4, lo que nuevamente sugiere el papel de una superficie de absorción reducida.
Esta técnica fue abandonada debido a la asociación con múltiples complicaciones graves a corto y largo plazo. Actualmente, la mayoría de los artículos publicados sobre este tema examinaron la necesidad de T4 en pacientes que se sometieron a un bypass gástrico en Y de Roux (BGYR), un procedimiento común. Al examinar a 23 pacientes, Raftopouloset al. ( 178 ) observaron que 13 de ellos mantuvieron el mismo requerimiento diario mientras que 8 mostraron una reducción de la dosis. Sin embargo, como se mencionó anteriormente, Sundaram et al. ( 132 ) y Fierabracci et al. ( 133 ) describieron que, cuando se normaliza por peso, es necesario aumentar la dosis de T4 para alcanzar los niveles de TSH objetivo en la mayoría de estos pacientes. Estos resultados están en consonancia con los valores elevados de TSH observados en pacientes tratados con la misma dosis de T4 antes y después de la cirugía ( 170 , 180 ). Se han realizado dos estudios farmacocinéticos para investigar este problema ( 130 , 181). A pesar de una mejora de los parámetros de absorción, Rubio et al. ( 181 ) observaron un retraso significativo en la absorción de T4 en los pacientes tratados quirúrgicamente. En el estudio mencionado anteriormente ( 130 ), los parámetros farmacocinéticos fueron similares antes y después de la cirugía de BGYR. Este último estudio también examinó a 15 pacientes a los que se les realizó derivación biliopancreática, observándose una mejora de los parámetros farmacocinéticos de T4 ( 130 ). Sin embargo, Fallahi et al. ( 180), al utilizar la misma dosis de formulación en tabletas de T4 antes y después de la cirugía, observaron que la TSH sérica empeoró después de la cirugía. Aunque los resultados en pacientes tratados exclusivamente con procedimientos malabsortivos coincidieron en identificar un claro aumento del requerimiento de T4, los resultados sobre las necesidades de T4 en pacientes tratados con procedimientos que combinan técnicas restrictivas y malabsortivas son contradictorios. Esto puede depender del diferente programa de ingestión de T4 (a menudo omitido) ( es decir , el tiempo de retraso entre la comida y la terapia u otros medicamentos) y de los diversos efectos que la cirugía puede tener en la fisiología gastrointestinal de un paciente ( p. ej ., alteración de la acidez del jugo gástrico, síndrome de dumping, retraso en el vaciado gástrico, diferente flora microbiana intestinal, variaciones en la proporción de masa corporal magra y grasa) (182 , 183 ). Además, la valoración de las necesidades de T4 no siempre normalizadas por peso no permite una comparación correcta y completa de los datos. La heterogeneidad de estos estudios en pacientes intervenidos de cirugía bariátrica con técnicas mixtas restrictivas y malabsortivas no permite sacar conclusiones definitivas sobre el efecto neto sobre el requerimiento de T4.
Uso de la Malabsorción de T4 como Herramienta para el Diagnóstico de Trastornos Gastrointestinales Ocultos
Un programa ajustado de tratamiento con T4 representa un requisito previo para detectar cualquier necesidad creciente de T4. Los pacientes que requieren una dosis de T4 superior a la esperada para alcanzar el objetivo de TSH pueden incluirse en la definición de “pacientes difíciles” según Ward. Están expuestos a hipotiroidismo refractario ( 3 ), pero no todos presentan malabsorción gastrointestinal. Una vez que se determina la existencia de una mayor necesidad de T4, el médico primero debe descartar pseudomalabsorción, peso reciente y significativo, índice de masa corporal y/o variaciones en la composición corporal, así como la posibilidad de embarazo. Luego, se debe realizar una cuidadosa anamnesis nutricional y farmacológica. Una vez que estos problemas se hayan descartado positivamente y se pueda sospechar razonablemente de trastornos gastrointestinales, se debe iniciar un estudio de diagnóstico.
Los antecedentes clínicos deberían ayudar en la estrategia diagnóstica, particularmente cuando la anemia ferropénica refractaria está presente simultáneamente: este tipo de anemia, de hecho, a menudo se asocia con infección por H. pylori, EC y gastritis atrófica, previa a la anemia perniciosa. La gastritis atrófica y la EC se asocian a su vez con frecuencia con hipotiroidismo autoinmune en el síndrome autoinmune poliglandular tipo III, incluso en pacientes jóvenes. Una infección previa o activa por H. pylori debe ser desplegada como primera línea, ya que es el trastorno más prevalente. Se debe realizar una prueba de aliento con 14 C-urea o detección de antígeno fecal de H. pylori y la medición de anticuerpos contra H. pylori. Si es positivo, tras el tratamiento adecuado, se debe investigar la afectación de la mucosa gástrica mediante endoscopia con múltiples biopsias. Una vez que la H. pylori se ha excluido la infección, se deben investigar otras posibilidades midiendo los anti-PCA y la gastrinemia en ayunas.
Los niveles elevados de gastrina sérica y la presencia de anti-PCA respaldan la sospecha de una atrofia gástrica autoinmune, y nuevamente se recomienda encarecidamente realizar una endoscopia con múltiples biopsias del cuerpo gástrico y el antro. En presencia de anemia ferropénica y/o distensión abdominal y dolor y/o diarrea crónica, la EC merece atención. La evaluación de los anticuerpos antitransglutaminasa y los niveles de IgA sérica total pueden ayudar a diagnosticar la EC pero, una vez más, solo la endoscopia puede confirmar o descartar la presencia de esta enfermedad. Si la sospecha se relaciona con otros trastornos intestinales, el estudio de diagnóstico debe incluir algunas pruebas de aliento (lactosa, glucosa, lactulosa) capaces de detectar IL ( 228 ), sobrecrecimiento bacteriano ( 229 ) y/o tiempo de tránsito alterado en el intestino, respectivamente. Estas pruebas de aliento se han considerado herramientas confiables, útiles y seguras en el diagnóstico de mala digestión de carbohidratos, siendo también las herramientas menos invasivas para diagnosticar el sobrecrecimiento bacteriano del intestino delgado ( 230 ). Finalmente, se debe tener en cuenta un examen de heces cuando se sospecha parasitismo ( p. ej ., G. lamblia ). Muchos de los trastornos gastrointestinales descritos pueden ocurrir de forma oculta o incluso oculta (figura 2 ). En este caso, el trabajo de diagnóstico debe basarse en la prevalencia de cada enfermedad, teniendo en cuenta el historial médico del paciente y su familia. Un estudio de diagnóstico exitoso puede descubrir la gran mayoría de las causas gastrointestinales de una mala respuesta al tratamiento con T4, pero también sería útil para diagnosticar y tratar estos trastornos gastrointestinales silenciosos, pero no inofensivos. Desde este punto de vista, la malabsorción de T4 puede representar una herramienta para diagnosticar enfermedades gastrointestinales ocultas.

Perspectivas farmacológicas alternativas
Aunque la formulación de tabletas de T4 sigue siendo el estándar de oro en el tratamiento del hipotiroidismo, la parafernalia hormonal ha evolucionado. El “paciente difícil” como lo describe Ward ( 217 ) es probablemente más que una excepción en el tratamiento del hipotiroidismo. El avance más reciente relacionado con el tratamiento con T4 proviene de la creciente atención a las formulaciones orales alternativas: la preparación líquida y la cápsula de gelatina blanda. La cápsula de gelatina blanda contiene, en una cubierta exterior de gelatina, T4 disuelta en glicerina ( 23 ). Esta estructura garantiza una disolución rápida en el ambiente gástrico ácido ( 231 ). La formulación líquida está compuesta por T4, glicerina y etanol y su característica más importante es que no requiere disolución gástrica ( 16). Se llevó a cabo un estudio de bioequivalencia cruzado de dos vías en 84 sujetos sanos para comparar tabletas de T4, cápsulas de gelatina blanda y solución oral ( 21 ). Los parámetros farmacocinéticos medios no fueron estadísticamente diferentes entre estas formulaciones; sin embargo, se observó una absorción más rápida de la solución de T4 probablemente debido a la falta de la fase de disolución ( 21 ). Está más allá del alcance de la presente revisión analizar en detalle las ventajas y desventajas de las preparaciones alternativas de T4, que, sin embargo, se revisaron recientemente en otro lugar ( 232). En la presente revisión, analizamos los estudios sobre el posible uso de estas preparaciones alternativas en pacientes con trastornos gastrointestinales. En un estudio prospectivo en 31 pacientes con malabsorción de T4 relacionada con el estómago, tratados de manera estable con una preparación de T4 en tabletas y cambiados a T4 en cápsula blanda, la dosis efectiva de esta última preparación se redujo significativamente en aproximadamente dos tercios de los pacientes ( 233 ). Más recientemente, datos muy preliminares sugirieron que el cambio de la preparación de T4 en tabletas a cápsulas blandas en una dosis sin cambios mejoró la TSH incluso en pacientes que tomaron una píldora 30 minutos antes del desayuno ( 234 ). Además, la preparación de cápsulas blandas de T4 ayuda a superar el problema de la interferencia del café y/o PPI en el tratamiento con tabletas de T4 ( 235 , 236).
La ventaja obvia y más importante de la solución líquida de T4 es la posibilidad de administración en edad pediátrica ( 237-239 ) o en pacientes que no pueden tragar tabletas o cápsulas ( 232 , 240 ). En recién nacidos y lactantes con hipotiroidismo, la dosis diaria de T4 se calcula de acuerdo con la edad, y las tabletas de T4 generalmente se trituran y se administran con líquidos ( 238 , 239 ). En estos pacientes muy jóvenes, la formulación líquida de T4 se maneja y administra fácilmente y también puede absorberse mejor que la formulación en tabletas ( 239 ). Las guías de la Sociedad Europea de Endocrinología Pediátrica reconocen esta alternativa de tratamiento en la edad pediátrica ( 241). En pacientes adultos con hipotiroidismo, algunos estudios analizaron si las restricciones del tratamiento con tabletas de T4 pueden superarse con el uso de esta preparación, es decir, si los alimentos pueden interferir con la absorción de T4 líquida como lo hacen con la formulación de tabletas ( 242 , 243 ). Un ensayo cruzado, doble ciego, aleatorizado, controlado con placebo sugirió que una formulación líquida de T4 podría ingerirse directamente en el desayuno, lo que podría mejorar el cumplimiento terapéutico ( 243 ) al reducir uno de los principales problemas en el tratamiento con tabletas de T4: el impacto negativo del desayuno sobre la eficacia del tratamiento ( 31 , 36 , 37 , 40 , 243 , 244). La preparación de T4 líquida se probó incluso en pacientes con malabsorción gastrointestinal. De hecho, en un estudio observacional prospectivo, se demostró que la preparación líquida supera la malabsorción de T4 inducida por el aumento del pH gástrico debido al tratamiento con PPI ( 245 ) y por LI ( 246 ). De manera similar, en una serie de casos, se demostró que la formulación líquida oral podría evitar la alteración del pH debido a la gastritis atrófica en pacientes que todavía tenían hipotiroidismo cuando se los trató con tabletas de T4 ( 247 ). Como se discutió anteriormente, la malabsorción de fármacos es una preocupación potencial después de la cirugía bariátrica. En un estudio reciente, pacientes con hipotiroidismo, bien reemplazados con tabletas de T4 antes de la cirugía (13 BGYR, 4 derivaciones pancreáticas biliares), mostraron un aumento de TSH de 3 a 8 meses después de la cirugía (180 ); el cambio a T4 líquida, a la misma dosis, mejoró significativamente los valores de TSH también en pacientes con derivaciones pancreáticas biliares, lo que confirma estudios previos en pacientes sometidos a BGYR ( 179 ).
A pesar de algunos resultados alentadores en pacientes con malabsorción gastrointestinal, el análisis general de estos estudios reveló algunas limitaciones: todo el campo merece más estudios sistemáticos antes de sacar conclusiones definitivas ( 248 ).
Conclusión
La malabsorción gastrointestinal de T4 oral es más frecuente de lo que se creía anteriormente y puede explicar una fracción significativa del hipotiroidismo refractario. Por este motivo, una correcta individualización del tratamiento hormonal ayuda en la detección de la malabsorción gastrointestinal de T4. Aunque el sitio de absorción de T4 es el intestino delgado, el pH gástrico surge como un requisito previo importante para la eficacia del tratamiento con tabletas de T4. Una mayor necesidad de T4 debe inducir al endocrinólogo a iniciar un trabajo de diagnóstico, basado en las características clínicas y en la prevalencia de trastornos gastrointestinales.
A pesar del creciente número de estudios, algunas preguntas están lejos de ser aclaradas. Los mecanismos fisiopatológicos de la absorción de T4 a nivel intestinal aún no están completamente definidos, como lo demuestran varios pacientes en los que la causa de una mayor necesidad de T4 sigue sin estar clara. En particular, las vías de transporte intestinal, la contribución real del reciclaje enterohepático y el papel de la composición de la microbiota en la absorción de T4 en humanos son temas para futuros estudios.






No Comments